
Cегодня дентальная имплантация является передовым методом лечения стоматологических заболеваний различной этиологии, связанных с потерей зубов [Ахмадова М.А., Игнатов А.Ю., 2011]. Анализ рынка стоматологических услуг свидетельствует о том, что ежегодно в мире устанавливается более 2 млн. имплантатов, уже в 90-е годы прошлого столетия общее число таких пациентов достигло 30 миллионов человек. Количество устанавливаемых имплантатов с каждым годом растет во всех экономически развитых странах.
В России имплантология стала развиваться сравнительно недавно, но оказалась крайне востребованной областью в стоматологии. Сегодня практически каждая клиника (частная и государственная) предлагает данный вид стоматологической помощи, так как имплантация является незаменимой альтернативой во многих клинических ситуациях.
Научные наблюдения и исследования клиницистов демонстрируют хорошие результаты имплантации, позволяющей достичь полноценного восстановления жевательной эффективности, речеобразования и эстетики зубного ряда.
На фоне широкого внедрения дентальной имплантации в стоматологическую практику, расширение показаний к имплантации и, несмотря на лавинообразный рост количества устанавливаемых стоматологами имплантатов, не уменьшается, а по данным ряда авторов увеличивается количество осложнений [Акопян Г.В., Хачатрян А.Г., 2011].
Несмотря на то, что имплантация в последние годы отличается высоким уровнем успеха в раннем послеоперационном периоде, в научной литературе появляется все больше сведений о риске отдаленных осложнений. Воспаление тканей, окружающих остеоинтегрированный имплантат, является одной из основных проблем имплантологии [Соловьева А.М., 2010, Тлустенко В.П., Гильмиярова Ф.Н., Головина Е.С. и др., 2011]. В 2008 г. на рабочем совещании Европейской федерации пародонтологии на основе современной научной доказательной базы было выработано согласованное мнение об инфекционновоспалительных поражениях в области дентальных имплантатов. Предложено выделять периимплантационный мукозит и периимплантит. Мукозит в области имплантата — это воспаление окружающих мягких тканей без нарушения остеоинтеграции. Дентальный периимплантит — это воспалительная реакция тканей, окружающих остеоинтегрированный имплантат, сопровождающаяся потерей опорной кости. Диагноз периимплантита устанавливают на основании рентгенологически выявленных изменений кости в виде кратерообразной деструкции в окружности шейки и даже верхней трети имплантата (рис. 1, 2).
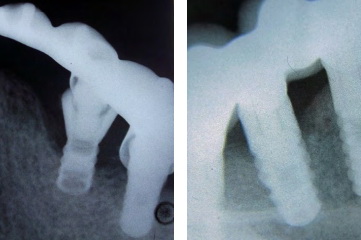
Рис. 1, 2. Рентгенологическая картина периимплантита.
Современные данные свидетельствуют о том, что мукозит может возникать у 80% лиц, имеющих дентальные имплантаты, а развитие периимплантита описано у 28—56% обследованных лиц [Lindhe J Meyle J., 2008].
Исследования последних лет свидетельствуют о том, что от 50 до 70 % пациентов с дентальными имплантатами страдают заболеваниями пародонта, что в отдаленном послеоперационном периоде может являться причиной потери зубов и имплантатов. Поэтому пациенты с ортопедическими конструкциями на дентальных имплантатах нуждаются в регулярном наблюдении не только хирурга-имплантолога, но и пародонтолога для предотвращения развития таких нежелательных воспалительных осложнений, как периимплатационный мукозит и периимплантит [Васильев А.В., Соловьева А.М., 2011].
Современные данные свидетельствуют о том, что мукозит может возникать у 60-80% лиц, имеющих дентальные имплантаты, а развитие периимплантита описано у 10—56% обследованных лиц [Zitzmann N.U., Berglundh T., 2011]. В нашей клинической практике подобные явления встречаются с частотой, соответствующей большинству данных научной литературы.
Патологические изменения вокруг имплантатов могут возникать как в ближайшие сроки после ротезирования, так и по прошествии нескольких месяцев и даже лет. Основными факторами развития осложнений в ближайшем послеоперационном периоде могут являться ошибки при выполнении хирургических процедур и проведения протезирования, тогда как основной причиной развития воспалительного процесса периимплантатных тканей в отдаленном послеоперационном периоде является несоблюдение пациентом графика регулярных посещений пародонтолога (гигиениста) или их отсутствие.
Главными факторами риска в развитии периимплантита являются отсутствие рациональной регулярной гигиены естественных зубов и ортопедических конструкций в полости рта и наличие в анамнезе пародонтита. Многочисленные микробиологические исследования демонстрируют, что функционирование имплантатов сопровождается развитием биопленок на внекостных поверхностях имплантата и протеза, а микробиота этой поддесневой биопленки сходна с таковой в пародонтальных карманах при пародонтите, при этом биопленка в трансмукозной (пришеечной) области супраконструкций имплантатов способна вызывать хроническое продуктивное воспаление в периимплантных такнях и привести к периимплантационному мукозиту и периимплантиту [Датдеева М.О., 2010]. Ключевая роль в развитии периим¬плантита принадлежит микрофлоре биопленки (рис. 3), представляющей собой сообщество микроорганизмов, сгруппированных в микроколонии, защищенных вырабатываемым ими липополисахаридным матриксом.
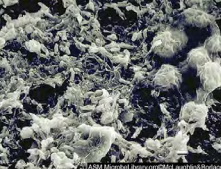 Рис. 3. Поддесневая биопленка.
Рис. 3. Поддесневая биопленка.
Причинно-следственная связь между накоплением микробной биопленки и развитием воспаления в тканях, окружающих имплантат, подтверждена в экспериментальных и клинических исследованиях [Heitz-Mayfield L.J., Lang M.A., 2000].
Развивишийся периимплантит, клиническая и микробиологическая картина которого сравнима с таковой при пародонтите, приводит к сокращению срока службы всей имплантационной конструкции.
Практически все авторы, в той или иной степени затрагивающие вопросы гигиенического ухода за полостью рта при имплантации, сходятся во мнении, что индивидуальная гигиена зубов, имплантатов и супраконструкций оказывает существенное влияние на стабильность искусственных опор, а от ее качества зависит срок службы имплантата и вероятность развития воспаления вокруг него [Roger Detienville, 2009]. Программа ухода за полостью рта после протезирования на внутричелюстных имплантатах базируется на основе индивидуальных особенностей ортопедической конструкции, строения челюстей и расположения зубов.
Обязательно обучение применению таких дополнительных средств гигиены как суперфлоссы, интердентальные ёршики, монопучковые зубные щетки, ирригаторы.
Гигиенические мероприятия, являющиеся неотъемлемой составляющей санации полости рта, при дентальной имплантации приобретают еще большее значение в связи с тем, что они способствуют снижению
риска осложнений и гарантируют долгосрочность успеха имплантации.
Имплантаты имеют тенденцию накапливать больше бактериального налета и плотных отложений, чем зубы. Вместе с тем, для проведения профессиональной гигиены в области имплантатов нет возможности использовать многие из традиционных доступных методов, в частности, нельзя применять обычные металлические ручные и ультразвуковые инструменты, нельзя полировать с использованием абразивных паст и циркулярных щеток и воздушно-абразивных методик с классическим порошком бикарбоната натрия, так как это может повредить структуру поверхности и повысить вероятность ретенции микробного налета.
Квинтессенцией развития воздушноабразивной технологии в стоматологии является появление безопасного абразива, которым можно работать под десной и полностью разрушить биопленку. Это порошок Air-Flow Perio® (EMS) глицин размером частиц 25 мкм, который вводится под десну (в отличие от обычной техники воздушно-абразивной обработки зуба бикарбонатом натрия, когда наконечник направлен от десны на расстоянии 3-5мм от поверхности зуба и 2 мм от края десны) при глубине кармана до 5 мм обычным наконечником Air-Flow или Air-Flow handy, при большей чем 5 мм глубине периимплантатного (пародонтального) кармана специальным наконечником Perio-Flow или Perio-Flow handy.
Механизм действия Perio-Flow® при работе над десной и до 5 мм под десной аналогичен методу Air-Flow -воздух из турбины поступает в шланг, далее в камеру с порошком, там равномерно смешивается с ним – получившаяся смесь идет к носику аппарата. В наконечнике два канала: по внешнему осуществляется подача воды, по внутреннему воздушно-порошковой смеси. Одновременно вода совершенно отдельно от порошковой смеси двигается к носику, где они выходят вместе, не смешиваясь, вода окружает оболочкой порошковую смесь, формируя (индуцируя) рабочую струю смеси, не давая распыляться ей в стороны, доводя ее до поверхности зуба. Водно-воздушная струя с тонкодисперсным чистящим порошком, сила которой регулируется в зависимости от индивидуальной клинической ситуации удаляет биопленку (рис. 4).
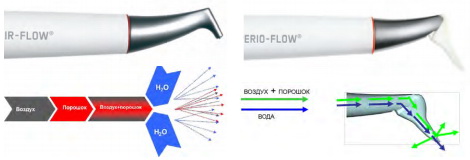
Рис. 4. Механизм воздушно-абразивного метода Perio-Flow® над десной (слева) и субгингивально (справа).
Субгингивальная обработка при глубине периимплантатного кармана более 5 мм проводится при помощью наконечника Perio-Flow с одноразовым стерильным носиком Perio, обеспечивающим тройную конусообразную подачу - легкий доступ и циркуляцию порошка глицина, воздуха и воды (рис. 4). Форма насадки обеспечивает низкое динамическое давление воздуха. Одноразовые насадки гарантируют гигиеничность. Мягкое применение биокинетической энергии оригинального метода Perio исключает риск повреждения десны и образования царапин на поверхности абатмента и имплантата, обеспечивает легкий доступ в любую зону 100% удаление биопленки без повреждений.
Дно периимплантатного кармана не повреждается, а полноценно очищается от биопленки, некротических масс и зрелых грануляций благодаря распылению порошка под давлением в трех плоскостях
и происходит успешное восстановление биосовместимости покрытых биопленкой поверхностей, за счет чего происходит уменьшение глубины периимплантатного кармана.
По данным [Schwarz F., Ferrari D., Popovski K. Et al., 2008] применение аквакинетической технологии Perio Flow (воздушно-абразивная над- и поддесневая обработка порошком глицина диметром частиц 25 мкм) (EMS, Швейцария) позволяет удалить 99,9 % биопленки, не повреждая поверхности имплантата.
Цель, материалы и методы исследования.
Для анализа клинической эффективности аквакинетического метода Perio Flow (EMS, Швейцария) в комплексном лечении пациентов с периимплантитом и периимплантатным мукозитом по сравнению с традиционными методами нами были изучены результаты лечения параимплантационных воспалительных заболеваний у 17 пациентов в возрасте 24-56 лет (9 мужчин и 8 женщин) – основная группа, и 5 пациентов – контрольная группа. Срок пользования имплантатами от 1-го года до 7-ми лет, имплантаты как во фронтальных участках, так и в области премоляров и жевательных зубов (всего 24 имплантата). Основная часть пациентов обратились с жалобами на кровоточивость, отделяемое из десны, дискомфорт, у части пациентов - 5 (29,4±0,7 %) периимплантит протекал бессимптомно и был диагностирован во время осмотра.
Диагноз периимплататный мукозит поставлен 2-м пациентам, у остальных – периимплантит, подтвержденный рентгенологически.
Контрольную группу составили 5 человек, этим пациентам проводилось стандартное лечение (профессиональная гигиена пьезоэлектрическим аппаратом PIEZON 700 (EMS), в области имплантатов - инструментом PI (EMS) (с пластиковым покрытием) (рис. 5), удаление налета неабразивными пастами механическим методом. Многоразовый, автоклавируемый инструмент PI, которым проводилась очистка имплантатов от зубных отложений, имеет запатентованное полиэфиркетонкетоновое покрытие, безопасное для поверхности имплантатов и керамики, работает с пьезоэлектрическим наконечником посредством присоединения через эндочак на 1200.
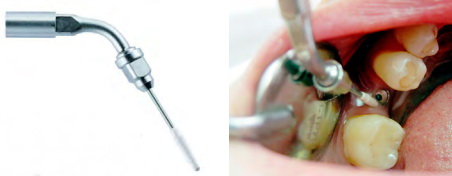
Рис. 5. Профессиональная гигиена имплантатов ультразвуковым методом специальным инструментом.
В основной группе, помимо стандартной профессиональной гигиены проводилось удаление биопленки методом субгингивальной аквакинетической обработки Perio Flow (EMS) на 2-й день (2-е посещение), через 6 недель (5-е посещение) (рис. 6).
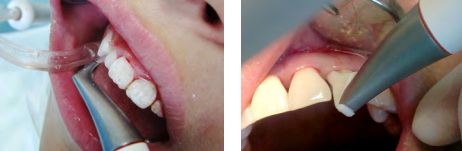
В комплекс лечения в обеих группах включались мотивация к рациональной гигиене полости рта (ГПР), обучение пациентов особенностям гигиены при наличии дентальных имплантатов с индивидуальным подбором основных и дополнительных средств гигиены, местная и (по показаниям) общая противомикробная и противовоспалительная терапия, витаминотерапия, местная иммунокоррекция, физиотерапия.
Оценка результатов проводимой терапии в каждой группе проводилась с помощью общепризнанных клинических методов - оценки глубины зондирования вокруг имплантата или периимплантатного кармана (ПИК), цвета периимплантатной десны, консиситенции, наличия или отсутствия экссудата из периимплантатной бороздки (кармана), величины периимплантатной маргинальной костной резорбции, упрощенного индекса гигиены полости рта (ГПР) OHI-S (J.C. Green, J.K. Vermillion, 1963), индекса для количественного определения налета в придесневой области Silness-Loe (S-L) (Silness J., Loe, H., 1964), индекса PMA (papillarmarginal-alveolar) (I.Schour, M.Massler, 1947, в модификации С.Parma, 1960).
По показаниям проводилась прицельная рентгенография. Анализ клинических параметров и индексную оценку проводили в каждое из посещений пациента (на 1-й, 2-ой, 5-й и на 10-й день, через 6 недель, через 3 и 6 месяцев) – всего 7 посещений.
Полученные результаты анализировались при помощи стандартных статистических методов.
Результаты исследования.
Обследование до лечения выявило высокие показатели индекса Silness-Loe (2,35±0,2 в основной и 2,28±0,1 в контроле) и OHI-S (2,81±0,22 и в основной и 2,65 ±0,51 в контроле) в обеих группах пациентов, что указывало на то, что практически у всех исследуемых на момент обращения была неудовлетворительная ГПР. Индекс PMA составил в среднем 58,5 ±2,8 % в основной и 57,3± 2,4 % в контрольной группах.
Согласно проведенным исследованиям, уровень ГПР (по значениям индекса OHI-S), изначально незначительно отличавшийся в обеих группах пациентов до лечения, на 5-й день (к 3-му посещению) в основной группе достиг 0,38 ± 0,33 и держался на этом уровне, в контрольной же группе уровень гигиены был хуже, и снизившись к 4-му посещению (через 10 дней) до 0,48 ± 0,27, через 6 недель составлял 0,53 ± 0,23 (p<0,001).
Уровень гигиены придесневой области согласно значению индекса Silness-Loe на фоне проводимой терапии значительно повысился на фоне инструктажа по гигиене и проводимой терапии в обеих группах, немного ухудшившись к 5-му посещению (через 6 недель), в последующие посещения же уже имелась разница в значениях индекса: в основной группе через 3 месяца – 0,92 ± 0,31, в контрольной – 1,96± 0,38(p<0,001) , через 6 месяцев в основной группе составлял 0,87 ± 0,11, а в контроле почти достиг исходного уровня – 2,14± 0,23 (p<0,001), несмотря на регулярный контроль с коррекцией гигиены.
В результате исследования установлено, что в процессе лечения состояние тканей десны вокруг имплантатов, характеризующееся индексом PMA улучшилось в обеих группах, оставаясь практически весь период лечения стабильным в основной группе: 12,1±0,8 - 11,7± 0,6- 11,9±0,9 в 5-е,6-е и 7-е посещения соответственно. В контрольной группе к 6-му и 7-му посещению ухудшилось по сравнению с результатом через 6 недель 13,6±1,7 - 16,9±1,3 - 17,8±2,1.
В результате проведенного лечения было зафиксировано уменьшение глубины ПИК в обеих группах. Причем в основной группе отмечена большая редукция глубины ПИК и через 6 недель, и через 3 месяца и через 6 месяцев (p<0,01) по сравнению с контролем (рис. 7).
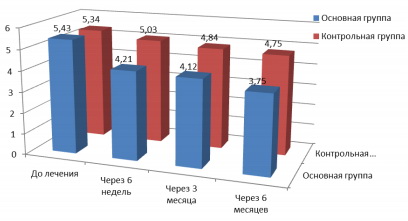
По данным клинического исследования нами установлено, что уже на 5-й день после начала лечения значения индекса придесневого налета, упрощенного индекса гигиены, пародонтального индекса значительно снизились. При этом различия между значениями изучаемых индексов до лечения и через 5 дней после его начала были статистически достоверными при анализе терапии с Perio Flow по сравнению с традиционным методом. Клиническими исследованиями подтверждалось уменьшение воспалительной инфильтрации в тканях десны около имплантатов. В основной группе с применением метода Perio Flow отмечалось более заметное и быстрое улучшение по ряду клинических показателей. В контрольной группе через 3 месяца и через 6 месяцев у некоторых пациентов наблюдался рецидив воспаления и ухудшение гигиенических показателей, что отражено в индексах. Пациентам провели снятие образовавшегося налета и были даны дополнительные инструкции по гигиене полости рта.
Сравнительный анализ двух методов по показателям редукции глубины ПИК выявил статистически достоверную наибольшую эффективность исследовательского метода по сравнению с контролем (p<0,01). Через 3 месяца и 6 месяцев от начала лечения исследовательский метод привел к более значительному уменьшению глубины ПИК по сравнению с методом, используемым в контрольной группе, что мы объясняем лучшим восстановлением биосовместимости тканей периимплантатного кармана во время аквакинетической обработки за счет разрушения биопленки по сравнению с традиционным способом.
Рекомендуемый нами для соблюдения график динамического наблюдения пациентов с дентальными имплантатами: через месяц после имплантации, далее каждые 3-4 месяца, при стойкой ремиссии – не реже 2-3 раз в год. При осмотре оценивается цвет, структура и консистенция десны, наличие гиперемии, отека и экссудата. При необходимости проводится легкое зондирование, также оценивается подвижность, фиксация протеза, наличие зубных отложений (индексы гигиены и при необходимости пародонтальные индексы: индекс кровоточивости, индекс распространенности воспалительного процесса). Рентгенография проводится, если есть патология и повторяется через каждые 12 месяцев, чтобы проверить уровень кости. После имплантации атрофия кости неизбежна, ее первичная потеря вокруг имплантата связана не с бактериями, по сути, являясь тканевым ответом на стоматологическое вмешательство, также может быть связана с излишней или недостаточной нагрузкой на еще не созревшую, полностью не минерализовавшуюся кость. В норме за первый год после операции потеря кости должна быть в пределах 1-1,5 мм, а затем замедлиться и составлять 0,2 мм каждый последующий год.
Учитывая этиопатогенетические аспекты периимплантита и свойства аквакинетического метода Perio Flow, наиболее перспективным звеном в комплексном лечении и профилактике периимплантита является применение безопасных для имплантатов методов удаления биопленки.
Применение аквакинетического метода в комплексном лечении пациентов с периимплантитом при соблюдении пациентом графика регулярных посещений пародонтолога в рамках поддерживающей пародонтальной терапии и постоянного контроля качества индивидуальной гигиены повышает клиническую эффективность традиционной терапии.