
директор Института Стоматологии
Национальной Медицинской Академии
Последипломного Образования им. П.Л. Шупика, г. Киев
Dr. Shterenberg А., к.м.н. B.Sc. Ph.D.,
практикующий хирург-стоматолог СНКЦ «Стамил»,
консультант и лектор компании «Стамил.Ру»
На сегодняшний день в современной хирургической стоматологии, челюстно-лицевой хирургии, пародонтологии, имплантологии для замещения и реконструкции костных дефектов используются различные остеотропные материалы.
Все эти материалы могут быть разделены на пять групп, исходя из источника их получения:
• аутогенные (донор – сам пациент);
• аллогенные (донор – другой человек);
• ксеногенные (донор – животное);
• аллопластические – полученные из природных минералов ( кораллы и т.п.);
• синтетические – на основе солей кальция и фосфора и других соединений.
Существуют четыре основные характеристики, которые должен демонстрировать любой костьзамещающий материал, чтобы считаться работоспособным. Эти характеристики представлены на Рис. 1.
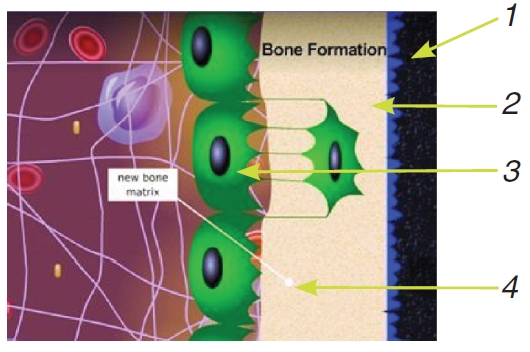
1 – остеоинтеграция – способность к химическому соединению с поверхностью имплантата или костной стенкой дефекта без вмешательства соединительной ткани;
2 – остеокондуктивность – способность обеспечивать формирование и рост костной ткани на своей поверхности;
3 – остеоиндуктивность – способность вызывать дифференцирование потенциальных мезенхимных клеток из окружающих тканей для образования остеобластов;
4 – остеогенез – способность формирования остеобластами новой костной матрицы в присутствии подсаженного материала.
Цель настоящей статьи – дать сравнительную характеристику используемых сегодня в стоматологической практике костьзамещающих материалов, оценить их преимущества и недостатки. Обосновать целесообразность применения синтетических костьзамещающих материалов, что позволяет уменьшить использование собственной и трупной кости в качестве остеотропного материала. Рассмотреть перспективы будущего синтетических материалов в реабилитации стоматологических больных.
Аутогенный костный материал
Аутогенный материал (собственная кость) обладает хорошо выраженными остеоиндуктивными свойствами. В то же время этот материал подвержен очень быстрой резорбции. При использовании его для заполнения костного дефекта или реконструкции альвеолярного отростка через полгода, как правило, 50% материала резорбируется остеокластами.
Забор собственной кости, довольно часто, сопровождается различными осложнениями: повреждением сосудов или нервов, образованием гематом или развитием воспалительных процессов. Следует помнить, что это всегда дополнительная операция, достаточно травматичная для пациента. Нужно также упомянуть и о том, что зачастую собственная кость резорбируется быстрее, чем наступает её интеграция и реконструкция дефекта [1].
Забор костного материала из внутриротовых участков часто приводит к инфицированию этих зон из-за присутствия в полости рта бактерий (Lambrecht et al. 2006) [17]. Мировые литературные источники убедительно отмечают, что при заборе собственной кости из подбородочной области в 20% случаев наступает парестезия, т.е. потеря чувствительности этой области.
Аллогенный костьзамещающий материал
Этот материал получают из кости другого человека. Его называют еще «трупная кость» или «деминерализованный лиофилизированный костный трансплантат». При использовании этого вида остеотропных материалов всегда существует определенная этическая проблема, связанная с согласием пациента на применение такого материала.
Костный аллотрансплантат характеризуется медленной остеоинтеграцией, показывает невысокий остеоиндуктивный потенциал и не участвует в остеогенезе, поскольку не содержит живых клеточных компонентов.
Его использование не исключает риск передачи различных заболеваний бактериальной или вирусной этиологии (гепатит В, С или ВИЧ ) от донора к реципиенту из-за реакции гистологической несовместимости и развития хронического гранулематозного воспаления [9].
Ксеногенные материалы
Эти материалы производятся не из человеческой кости. Основным источником получения ксеногенных материалов являются кости крупного рогатого скота (бычьи кости): (Bio-Oss, Cerabone, SmartBone). Иногда применяются кости свиньи (OsteoBiol -MP3, The Graft) или конские кости (Bioteck).
Костная матрица подвергается химической и физической обработке. Согласно инструкции производителя ответная реакция организма и передача заболеваний полностью исключены.
Однако, как контраргумент декларациям производителя, имеющиеся литературные источники, указывают на то, что даже в обработанной кости могут оставаться протеиновые фракции донорского организма (Schwartz et al. 2000) [24]. Опубликованы также предостережения относительно возможности прионового инфицирования. (Васильев А.В. Котова-Лапоминская Н.В. 2004) [1].
Ксеногенные костьзамещающие материалы достаточно хорошо научно и клинически изучены. Установлено, что они остаются включенными во вновь сформированную костную матрицу. Резорбция материала, содержащего бычью кость, не отмечалась даже через 11 лет. Исследователи отмечали крайне низкий уровень резорбции этих материалов в организме человека (Mordenfeld et al.2010) [18].
Ксеногенные материалы обладают как остеоиндуктивными, так и остеокондуктивными свойствами. Они не резорбируются полностью в организме и всегда требуют использования защитной мембраны.
Синтетические костьзамещающие материалы
На протяжении последних 30 лет были разработаны и внедрены в клиническую стоматологическую практику различные синтетические костьзамещающие материалы. Для заполнения костных дефектов используются такие искусственные костьзамещающие материалы как: Cerasorb (Germany); SintoGraft (USA); Maxresorb, BoneSigma BCP (USA); easygraft ®, easy-graft® CRYSTAL (Switzerland) и многие другие.
Идеальные синтетические костьзамещающие материалы должны быть биологически совместимыми, проявлять минимальную фиброзную реакцию и поддерживать формирование новой кости.
С точки зрения механической прочности синтетические костьзамещающие материалы должны иметь прочность близкую к прочности заменяемой кортикальной и губчатой костей.
Эти требования достигаются в том случае, когда модуль эластичности материала совпадает с модулем эластичности собственной кости. В таком случае есть возможность предотвратить возникновение стрессовых ситуаций, обеспечить адекватную прочность и предотвратить усталостные растрескивания имплантата при циклической нагрузке.
Синтетические материалы, которые демонстрируют некоторые из этих качеств, являются композициями соединений кальция, фосфора, кремния и алюминия.
Биоактивное стекло
Две группы материалов, в основе которых содержатся силикатные смеси, способны вступать в непосредственный контакт с костной тканью. Это – биоактивное стекло и стеклоиономеры.
Биоактивное стекло – это твердый, монолитный (непористый) материал, который впервые был описан еще в 1970-х годах. Биоактивное стекло состоит из окиси натрия, окиси кальция, пентоксида фосфора и диоксида кремния. Диоксид кремния, известный под названием «кремнезем», является основным весовым компонентом.
Изменяя соотношения окиси натрия, кальция и двуокиси кремния, можно создавать такие формы биостекол, которые будут более или менее растворимыми в организме (растворимость, главным образом, определяется содержанием окиси натрия) [11, 12].
Биоактивное стекло обладает как остеоинтегративными, так и остеокондуктивными свойствами. Механически прочное соединение между биоактивным стеклом и костной тканью образуется в результате того, что при контакте с жидкостью костной среды или раны, на поверхности биоактивного стекла формируется слой геля насыщенного кремнием. В среде этого геля, ионы Ca2+ и (PO4) 2вступают в реакцию, образуя кристаллы гидроксиапатита (НА) очень похожие на НА костной ткани, в результате чего наступает прочное соединение. [10,12].
Блоки из биоактивного стекла очень трудно просверлить или придать им какую либо форму. Они весьма хрупкие и часто ломаются при механической обработке. Следовательно, их очень сложно фиксировать к костной ткани.
Использование биоактивного стекла в виде гранул допускается в качестве наполнителя костного дефекта только в тех зонах, где не присутствует нагрузка. Следовательно, по сравнению с другими упомянутыми в статье материалами, данный материал не демонстрирует никаких преимуществ. Наоборот, многие материалы резорбируются быстрее чем НА, что обеспечивает более раннюю реставрацию костного дефекта [20]. Более успешное использование биоактивного стекла отмечается при его нанесении на поверхность имплантата, для увеличения остеоинтеграции титанового имплантата [23].
Разновидностью биоактивного стекла является биоактивная керамика
Биоактивная керамика имеет более высокую прочность и лучшие механические свойства по сравнению с биоактивным стеклом, однако оба эти материала имеют низкую прочность на излом по сравнению с кортикальной пластинкой костной ткани. Они хрупкие и склонны к переломам, особенно при действии циклических нагрузок, что в значительной степени сужает область их применения в стоматологии.
Стеклоиономеры
Стеклоиономерные цементы были впервые представлены для использования в стоматологии в 1971 г., когда потребовался цемент способный работать во влажной среде. Один из таких цементов, предназначенных для замещения костных дефектов, описывался в работе [16].
Порошок этого цемента, представляющий собой измельченное стекло, содержащее оксиды кальция, алюминия, кремния и фторсиликаты, с диаметром частиц от 0.001 до 0.1 мм, смешивался с поликарбоксилатной кислотой. В результате этого смешения происходила экзотермическая реакция с выделением CO2, приводящая к образованию пористой пасты цемента.
Паста твердела приблизительно через 5 минут после чего цемент становился нерастворимым в воде. Однако, на протяжении всего времени отверждения, такой цемент должен быть защищен от попадания влаги, которая растворяет не успевшую прореагировать поликарбоксилатную (полиакриловую) кислоту.
Стеклоиономерный цемент – биологически совместимый материал, обладающий свойствами остеоинтеграции, что в, некотором смысле, делает его подобным биоактивному стеклу. Его пористость придает цементу остеокондуктивные свойства, способствуя прорастанию костной ткани.
Следует отметить, что стеклоиономерный цемент не резорбируется и не замещается на собственную кость.
Продолжение следует...