
О.А. Гуляева,
к.м.н., асс. кафедры стоматологии общей практики ИПО БГМУ,
член Международной эндодонтической федерации,
Европейского эндодонтического общества,
авторизованный лектор Swiss Dental Academy в России
Воспалительные процессы в тканях пародонта являются доминирующими в структуре хронических стоматологических заболеваний. На сегодняшний день воспалительные заболевания пародонта (ВЗП) до сих пор продолжают оставаться наиболее массовыми, повсеместными заболеваниями взрослого населения, серьезно воздействуя на состояние его здоровья, снижая его трудоспособность и качество жизни [Чобанов Р.Э., Мамедов Р.М., 2010].
По данным Всемирной организации здравоохранения распространенность ВЗП у лиц старше 40 лет превышает 95 % [Омаров И.А. и др., 2011] и является основной причиной потери зубов в возрасте 40-65 лет [Непомнящая Н.В. и др., 2010]. Значительный рост распространенности заболеваний пародонта, тенденция к длительному хроническому течению и рецидивам, появление тяжелых и быстропрогрессирующих форм, зачастую недостаточная эффективность проводимого лечения, включая хирургические методы [Земерова Д.В. и др. 2012, Цепов Л.М., 2009], прогрессирующее течение процесса деструкции костной ткани, ведущее к потере зубов [Соболева Л.А. и др., 2010], заставляет стоматологов всего мира уделять пристальное внимание проблеме их профилактики и лечения.
Высокая медико-социальная значимость ВЗП обусловлена также их вкладом в развитие метаболического синдрома, гипертонической болезни, ишемической болезни сердца, занимающих важные позиции в структуре причин инвалидизации и смертности населения [Горбачева И.А., 2008]. Стремительное развитие пародонтологии в последние годы, обогащение ее новыми научными знаниями, уточнение многих звеньев патогенеза и особенностей клинического проявления воспалительных заболеваний пародонта, непрерывная разработка новых методов диагностики, средств для лечения, говорит об остроте проблемы ВЗП и актуальности поиска новых методов для их терапии.
Основным причинным фактором возникновения ВЗП с уверенностью можно назвать микроорганизмы биопленки [Eick S., Bender P., Flury S. at al., 2012]. Уровень знаний об этиологии и патогенезе воспалительных заболеваний пародонта заставляет признать бактериальную модель возникновения и течения заболевания как одну из причин, которую необходимо рассматривать в комплексе с индивидуальной реакцией организма человека и воздействием внешних факторов.
Современной концепцией пародонтологического лечения и профилактики ВЗП является минимизация воспалительных реакций путем оптимизации контроля поддесневой биопленки – структурированного сообщества бактериальных пародонтопатогенов, инкапсулированных в самопродуцируемую полимерную матрицу, служащим барьером от антимикробных средств общего и местного действия. Биопленка характеризуется поверхностным прикреплением, неоднородной структурой, генетическим многообразием, сложными внутрисистемными взаимодействиями [Кисельникова Л.П., 2010]. В природе биопленки распространены повсеместно. Установлено, что свыше 95% существующих в природе бактерий находятся в биопленках. Биопленки выстилают постоянные катетеры, внутренние имплантаты, контактные линзы и протезы. Биопленки могут оказаться смертоносными. Болезнь легионеров, унесшая жизни 29 человек в Филадельфии в 1976 г., в конечном счете, оказалась связанной с бактериями биопленки в системе кондиционирования воздуха. Миллионы долларов ежегодно расходуются на работы по контролю за этими биопленками.
Об эффективности технологий воздействия на поддесневую биопленку в комплексе первичного пародонтального лечения в современной научной литературе имеется много подтверждений. По данным ряда авторов эти методы, в частности из доступных российскому врачу, воздушно-абразивная субгингивальная терапия взвесью глицина – Perio-Flow® (EMS, Швейцария) является целенаправленным щадящим способом минимально инвазивной терапии, позволяющей добиться разрушения биопленки, что имеет решающее значение для успеха лечения [Flemmig T.F., 2007, Petersilka G., 2008].
Цель работы: оценить эффективность технологии Perio-Flow (EMS, Швейцария) для удаления биопленки в комплексном лечении пародонтита, сравнить ее с традиционными методами и проанализировать ее влияние на степень редукции глубины пародонтальных карманов.
Материалы и методы исследования
Группу исследования составили 55 пациентов с пародонтитом средней степени тяжести в стадии обострения в возрасте 35 – 44 года. Для анализа результатов проводимой терапии оценивали упрощенный индекс гигиены полости рта (ГПР) OHI-S (J.C. Green, J.K. Vermillion, 1963), индекс для количественного определения налета в придесневой области Silness-Loe (S-L) (Silness J., Loe, H., 1964), индекс кровоточивости десен PBI (Saxer & Muhlemann, 1975), эффективность лечения определяли по индексу Улитовского:
Эффективность (в %) = 100*(PMA1 – PMA2)/PMA1,
где PMA1 - индекс PMA (papillar-marginalalveolar) (I.Schour, M.Massler, 1947, в модификации С.Parma, 1960) до лечения, PMA2 – после лечения.
Глубину пародонтального кармана (ПК) определяли с помощью стандартной методики, делая по 3 измерения с вестибулярной и небной поверхности 6-ти зубов у каждого из пациентов (1.6, 2.5, 2.6, 3.6, 3.1, 4.6), пародонтальным калибровочным зондом (D=0,5мм) со стандартным давлением 240 N/см, регистрируя глубину с точностью до 1 мм. Индексная оценка проводилась в каждое из посещений пациента (на 1-й день, на 2-ой день, на 5-й день, на 10-й день, через 6 недель, через 3 месяца) – всего 6 посещений, глубину ПК определяли в 1ое, 5-ое и 6-ое посещение.
В комплекс лечения включались мотивация и обучение пациентов гигиене полости рта (ГПР), общая и местная противомикробная и противовоспалительная терапия, витаминотерапия, местная иммунокоррекция. В 1-ой группе исследования (контрольной – 15 человек) – проводилось снятие твердых зубных отложений (ЗО) при помощи ультразвукового пьезоэлектрического аппарата Piezon® Master 700 (EMS, Швейцария) и налета (ЗН) воздушно-абразивным аппаратом Air-Flow® Master (EMS, Швейцария) порошком Air-Flow® Classic (гидрокарбонат натрия, диаметр частиц 65 мкм) или порошком Air-Flow® Soft (глицин, диаметр частиц 65 мкм) при наличии гиперестезии, рецессий десны, клиновидных дефектов, во 2-ой (30 человек) – ЗО и ЗН снимали ультразвуковым и аквакинетическим способом, (как в 1-ой группе), кроме этого удаляли субгингивальный налет (биопленку) при помощи аппарата Air-Flow® Master (EMS, Швейцария) порошком Air-Flow® Perio (глицин, диаметр частиц 25 мкм) (рис. 1).
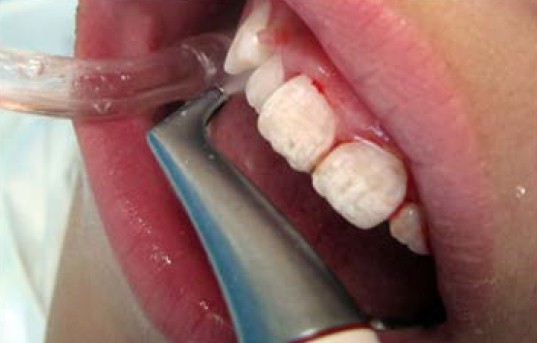
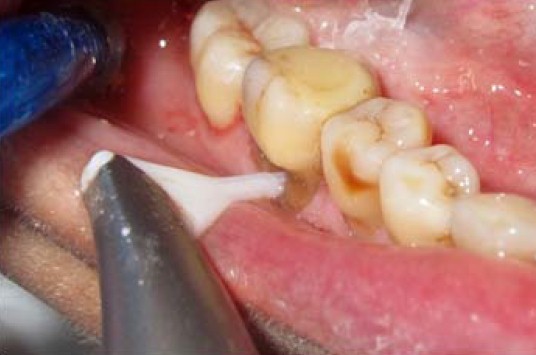
Рис 1. Очистка пародонтальных карманов от биопленки Perio-Flow при глубине до 5 мм обычным наконечником Air-Flow порошком Perio, более 5 мм наконечником Perio-Flow со специальным стерильным пластиковым носиком Perio-Flow Nozzle.
Процедуру удаления биопленки проводили 2 раза за время исследования (на 5-й день и через 6 недель) и сравнивали уровень редукции глубины пародонтальных карманов после лечения в динамике (3 месяца). При обработке полученного материала использовались стандартные статистические методы.
Результаты исследования
До начала лечения гигиенический и пародонтологический статус пациентов во всех группах был примерно одинаков: индекс кровоточивости PBI в среднем составлял 3,6±0,03, неудовлетворительная гигиена полости рта подтверждалась высокими показателями индекса гигиены полости рта Silness–Loe (2,87±0,06) и OHI–S (2,3±0,08). Глубина ПК варьировала от 3 до 5 мм, индекс PMA составил в среднем 58,5 ±2,8 %. У всех пациентов во время лечения заметно улучшилось гигиеническое состояние полости рта, о чем свидетельствует редукция индекса OHI–S на 10 день в 4,6 раза (0,5±0,02) и в 2,6 раза (0,9±0,03 – удовлетворительная гигиена) через 6 недель после лечения с незначимой разницей в обеих группах. Динамика редукции индекса придесневого налета имела различия в группах исследования: на 4-ое посещение – наивысшая степень редукции была получена во 2-ой группе – 82,2±0,8% , в контроле 59,4 ±0,4 % и разница становилась более значительной на протяжении периода наблюдения (рис. 2).
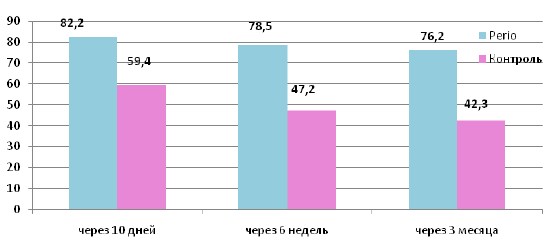
Рис 2. Степень редукции индекса Silness-Loe через 10 дней, 6 недель и 3 месяца от начала терапии, %.
Так как гигиена над десной (согласно индекса OHI-S) после коррекции гигиенических навыков и проведения профессиональной гигиены одинакова, то разница в индексе придесневого налета S-L, по нашему мнению, обусловлена результатом полноценного удаления поддесневого налета и биопленки Perio-FLOW, что позволило устранить микронеровности, достичь максимальной гладкости поверхности и уменьшить риск ретенции зубного налета и образования зубных отложений.
Наблюдалась положительная динамика по индексу кровоточивости, коррелирующая с индексом придесневого налета. Разница в степени редукции папиллярного индекса кровоточивости PBA показала большую эффективность в снятии клинических симптомов воспаления при комплексном лечении с использованием разрушения биопленки (рис. 3).
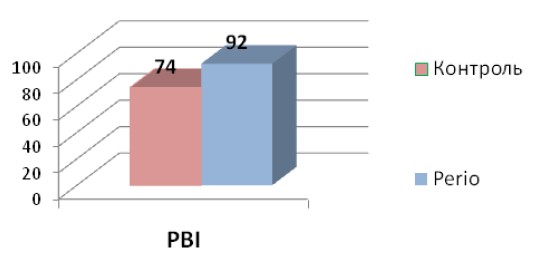
Рис 3. Степень редукции показателя воспаления – индекса кровоточивости десен PBI на 3-е посещение через 5 дней от начала терапии, %.
После базового курса лечения на 10-й день индекс PMA снизился в 4,7 раза по сравнению с исходным значением в основной группе и в 3,2 раза в контрольной (p<0,01). (рис. 4).
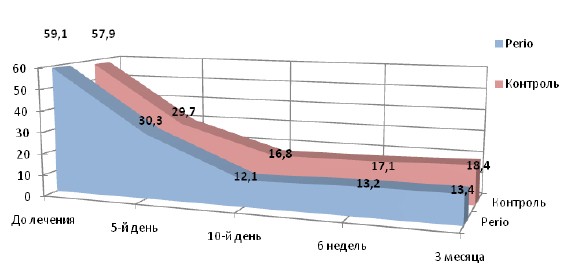
Рис 4. Динамика снижения воспалительных явлений в тканях пародонта (согласно индекса PMA) на фоне проводимой терапии.
Эффективность лечения, согласно индекса Улитовского, была лучшей и более стабильной как после базового курса (через 10 дней), так и в отдаленные сроки (через 3 месяца) в группе, где удаляли биопленку (рис. 5).
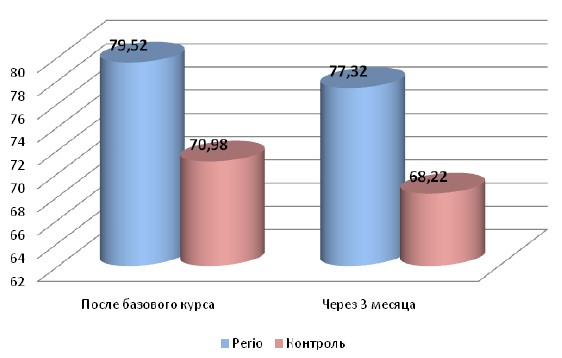
Рис 5. Динамика индекса эффективности Улитовского в группах исследования в течение периода наблюдения, %.
В результате консервативного лечения пациентов со средней степенью тяжести пародонтита глубина пародонтальных карманов уменьшилась на 17,5±3,5% (на 0,73±0,08 мм) (p<0,01) в группе с применением поддесневой обработки Perio-Flow, а в контрольной – всего на 8,2 ± 1,3 % (0,24±0,04 мм) (таб. 1).
Выводы и практические рекомендации
Объективные данные гигиенических, пародонтальных индексов и клинических показателей процессов регенерации в период наблюдения доказали преимущества использования современной малоинвазивной технологии Air-Flow® Perio для удаления биопленки в комплексе профессиональной гигиены по сравнению с традиционными методами.
Методы удаления биопленки в современной стоматологии в комплексе проведения пародонтальной терапии являются перспективным методом профилактики воспалительных заболеваний пародонта, в некоторой степени альтернативой существующим на сегодняшний день традиционным (хирургическим) методам редукции глубины пародонтальных карманов и выходом для пациентов, имеющим тем или иные противопоказания для проведения хирургического вмешательства: беременность, аллергия, серьезная соматическая патология, сниженный иммунитет и регенераторные способности, пожилой возраст, страх перед инвазивными методами лечения и т.д.
Полученные в ходе проведенных исследований результаты позволяют рекомендовать к широкому применению в практике врачей-пародонтологов и врачей-гигиенистов методы удаления биопленки в качестве дополнения к профессиональной гигиене для повышения качества консервативного лечения и эффективной профилактики воспалительных заболеваний пародонта.
Разработанная на основе исследований и наблюдений, оправдавшая себя результатами на клиническом приеме схема, рекомендуемая для практического применения Perio-Flow: 1-я процедура субгингивального разрушения биопленки после профессиональной гигиены в течение противовоспалительного курса (либо в 1-ое посещение сразу – индивидуально), 2-я процедура – через 2-7 недель (индивидуально, в среднем через месяц), 3-я процедура – через 2,5-4 месяца, далее через 5-6 месяцев. При констатации ремиссии - поддерживающая терапия: при тяжелой степени пародонтита – 3-4 раза в год, при средней – 2-3 раза в год, при легкой – 1-2 раза в год, индивидуализация сроков и количества процедур в зависимости от клинической ситуации.
ВНИМАНИЕ! Любое копирование и размещение в сторонних источниках материалов, опубликованных на сайте WWW.STOMPORT.RU, возможно только при указании АКТИВНОЙ ссылки на источник. При копировании этой статьи указывайте: